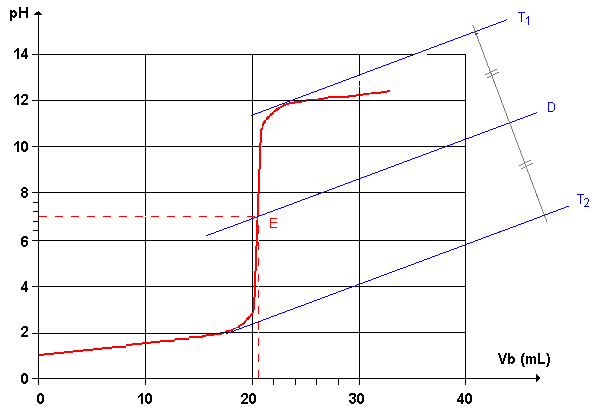
dosage d'un acide fort par une base forte
1- nature de dosage :
la courbe pH = f (vb ajoutée) admet un seul point d'inflexion de même pH équivalence (pHE) égale à 7
d'ou elle correspond au dosage d'un acide fort par une base forte
2- équation de la réaction :
H3O+ + OH- = 2 H2O
3- Montrer que cette réaction est totale :
k = 1/Ke = 10 à la puissance 14 > 10 à la puissance 4
d'ou cette réaction est totale
4- équivalence acido _basique :
définition :
à l'équivalence acido_ basique est obtenu lorsque le nombre de mol initial d'acide égale au nombre de mol de base ajoutée à l'équivalence
CA VA = CB VBE
5- Nature de milieu à l'équivalence :
méthode 1 :
à l’équivalence le milieu est neutre car pH = 7
méthode 2 :
les entités chimiques présentent à l'équivalence sont Na+ , CL- , H3O+ , OH- et H2O
or NA+ et CL- sont des ions inertes et la concentration de H3O+ est égale à celle de OH-d'ou le milieu est neutre
6- Choix de l'indicateur coloré :
l'indicateur coloré le mieux adapté pour ce dosage est le BBT car pHE appartient à sa zone de virage
la courbe pH = f (vb ajoutée) admet un seul point d'inflexion de même pH équivalence (pHE) égale à 7
d'ou elle correspond au dosage d'un acide fort par une base forte
2- équation de la réaction :
H3O+ + OH- = 2 H2O
3- Montrer que cette réaction est totale :
k = 1/Ke = 10 à la puissance 14 > 10 à la puissance 4
d'ou cette réaction est totale
4- équivalence acido _basique :
définition :
à l'équivalence acido_ basique est obtenu lorsque le nombre de mol initial d'acide égale au nombre de mol de base ajoutée à l'équivalence
CA VA = CB VBE
5- Nature de milieu à l'équivalence :
méthode 1 :
à l’équivalence le milieu est neutre car pH = 7
méthode 2 :
les entités chimiques présentent à l'équivalence sont Na+ , CL- , H3O+ , OH- et H2O
or NA+ et CL- sont des ions inertes et la concentration de H3O+ est égale à celle de OH-d'ou le milieu est neutre
6- Choix de l'indicateur coloré :
l'indicateur coloré le mieux adapté pour ce dosage est le BBT car pHE appartient à sa zone de virage
extrait du cours fait par MR : BEN HAJ MOUNIR